近日,甫康药业CVL009片治疗EGFR罕见突变晚期非小细胞肺癌的单臂、开放、多中心临床研究项目启动会顺利举行,标志着公司CVL009项目正式进入临床实施阶段。甫康药业临床运营团队在吴子爱副总裁领导下,一直期盼着该项目尽早启动,大家提前做足准备,争分夺秒,有条不紊地开展各项工作:3月30日提交IND申请,6月12日获得临床批件,在短短2个月内获得全国8家知名三甲肿瘤医院肺癌教授们的大力支持,6月获得中心伦理批件并且完成了数十家供应商合作伙伴的签约,非常高效地完成了各项准备工作,为即将到来的临床试验患者顺利入组打下了坚实的基础。
甫康药业CEO沈孝坤博士表示中国肺癌患者基数庞大,肺癌罕见基因突变患者的临床需求不容忽视。目前国内EGFR罕见突变晚期非小细胞肺癌还没有靶向治疗药物获批上市,患者亟需更好的治疗方案。CVL009片一旦获批上市将为中国EGFR罕见突变晚期非小细胞肺癌患者提供疗效好、可负担的治疗选择,希望大家共同努力早日完成临床试验和注册上市工作。临床运营副总裁吴子爱女士在致辞中表示:一个高质量的注册临床试验顺利完成需要团队高效协作,我们将共同应对挑战,实现预定目标。本项目成功上市将会为晚期肺癌患者带来最先进的治疗方案,也将改变中国患者治疗指南。启动会上高级医学经理王琼和项目经理王东分别介绍了临床研究方案设计和项目管理工作计划。通过本次会议,大家明确了各自的任务和职责,团队成员建立了完善的项目管理会议机制,明确了研究时间表。大家一起对研究过程中可能遇到的潜在困难进行了充分的分析和讨论,纷纷表示要竭尽全力,保质保量完成任务。
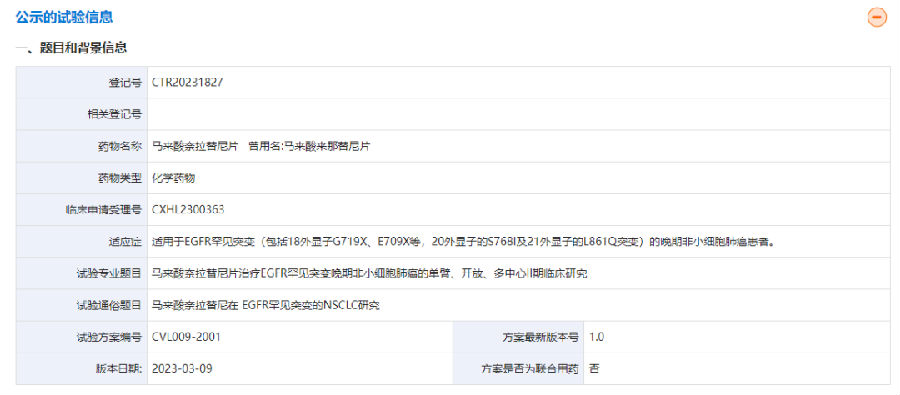
该项目在全国8家知名医院研究中心同步开展:
